���F�ڵ�λ�ã� �ٝ�����ˎ���W��� >> �� >> ����
�Ї�����ɭ���ί�ָ�ϣ������棩
- ��Դ�� �ٝ�ˎ��ˎӍ ���ߣ��ٝ��ӑB �g�[�� �l���r�g��2014/8/5 15:36:00
����ɭ����Parkinson’sdisease����һ�N��Ҋ����������ϵ�y�����Լ�������Ҫ�Ժ��|��Ͱ�����Ԫ�M������׃��·��С�w�γɵIJ���׃�����y���w�^��Ͱ��f�|���͡���Ͱ��c����đ�A�f�|ʧƽ���������׃���������ֱ�������t�����˄�ƽ���ϵK���\�ӰY������X�p�ˡ�������˯���О鮐���������ȷ��\�ӰY����R�����F���@��������
�҇� 65 �q������Ⱥ���w�����ʞ� 1700/10 �f�����S���g���L�����ߣ��o��ͥ������������˳��ص�ؓ������Щ������oՓ�nj�����ɭ���l���C�Ƶ��J�R�Լ��������\������W��־��İl�F��߀�nj����ί��������ֶε�̽�����������@�����M�������������ǚW�����ҵ�����ɭ���ί�ָ�Ͻo�����҂��ܺõĆ�ʾ�͎�����
���A�t�W�����W�֕�����ɭ�����\���ϵK�W�M�� 2006 ��� 2009 ��քe�ƶ��˵�һ�������Ї�����ɭ���ί�ָ�ϣ���Ҏ���̓����҇�����ɭ�����ί��О������ί�Ч����������Ҫ�����á��� 5 ��������ȡ�����ԓ�ί��I��������һЩ�ί�����ĸ��º��ί��������M����
���˸��õ��m����lչ�Լ����õ�ָ���R�����`���҂��F���Ї�����ɭ���ί�ָ�ϵڶ����M�б�Ҫ���ĺ��¡�
1. �ί�ԭ�t
1.1 �C����
ÿһ������ɭ�����߶������Ⱥ��ͬ�r���F���\�ӰY��ͷ��\�ӰY��������������ж��������@��Y��Еr���a����N���\�ӰY����H�\�ӰY��Ӱ��˻��ߵĹ����������������������\�ӰY��Ҳ���@�ɔ_�˻��ߵ������|������ˣ��҂���ԓ������ɭ�����\�ӰY��ͷ��\�ӰY���ȡȫ��C�ϵ��ί���
�ί��������ֶΰ���ˎ���ί������g�ί����\�ӯ����������茧�������o���ȡ�ˎ���ί������x�����������ί��^���е���Ҫ�ί��ֶΣ����g�ί��t��ˎ���ί���һ�N��Ч�a�䡣Ŀǰ���õ��ί��ֶΣ��oՓ��ˎ������g�ί���ֻ�ܸ��ƻ��ߵİY���������ֹ����İlչ�����o����������ˣ��ί����HҪ���㮔ǰ��������Ҫ�L�ڹ��������_���L�ګ@�档
1.2 ��ˎԭ�t
�������\�ӰY��ͷ��\�ӰY���Ӱ푻��ߵĹ������ճ�������������ˣ���ˎԭ�t��ԓ���_����Ч���ưY���߹��������������|����Ŀ�ˡ��҂��ᳫ�����\�ࡢ�����ί������H���Ը��õظ��ưY����ҿ��ܕ��_���Ӿ������Mչ��Ч����
���Գ�“�����ζ�”�Ա���a��ˎ��ļ��Ը����ã����F“�M������С�����_���M���R��Ч��”����ˎԭ�t��������\�Ӳ��l�Y�����Ǯ��ӰY�İl���ʣ����C���҇�����ɭ�����ߵĮ��ӰY�l�������@���ڇ��������ɭ�����ߡ�
�ί�����ѭѭ�C�t�W���C����Ҳ�����{���w�����c����ͬ���ߵ���ˎ�x����Ҫ�C�Ͽ��]���ߵļ������c�������������߀���ԏ�ֱ�لӞ������ͼ������س̶ȡ��Пo�J֪�ϵK���l�����g���͘I��r���Пo������ˎ����ܵĸ����á����ߵ���Ը�������������������أ��M���ܱ��⡢���t��p��ˎ��ĸ����ú��\�Ӳ��l�Y��
�M�п�����ɭ��ˎ���ί��r���e��ʹ��������͕r����ͻȻͣˎ������l����ˎ���ԾC������
2. ˎ���ί�
�����R���Y����ضȵIJ�ͬ�����Ԍ�����ɭ���IJ��̷֞����ں������ڣ����� Hoehn-Yahr1~2.5 �����x�����ڣ�Hoehn-Yahr3~5 �����x�������ڡ������҂��քe�����ں� ����������ɭ��������w���ί���Ҋ��
2.1 ��������ɭ�����ί� ����һ���l�����S���r�g�����ƶ��u�M�Լ��أ����C����ʾ�ڼ��������A�εIJ����Mչ�^�����A��Ҫ�졣��ˣ�һ�������\�࣬�����M���_ʼ�ί�����ȡ���ռ�������r�C�����������ɭ���������ί��ɔ����P�I�����á�
�����ί����Է֞��ˎ���ί��������J�R���˽⼲�����a��I�B���ӏ�呟����Զ����ټ����������Լ�����ͼ��ˌ����ߵ����⡢�P���c֧�֣���ˎ���ί���һ�㼲�����ڶ����ˎ�ί�����Ҳ�ɲ��Ã�����С������Nˎ��w�F����c�����ϑ��ã������_����Ч��ѡ��S�֕r�g���L���\�Ӳ��l�Y�l������͵�Ŀ�ˡ�
ˎ���ί�������������ί�ˎ��ͰY�����ί�ˎ���������ί�ˎ����˿��ܵļ�����������⣬Ҳ���и��ưY������ã��Y�����ί�ˎ������܉����@���Ƽ����Y���⣬����Ҳ����һ���ļ���������á�
��������ί���Ŀ�����Ӿ��������Mչ��Ŀǰ���R���Ͽ����м���������õ�ˎ����Ҫ�����ΰ�����ø B �ͣ�MAO-B�����Ƅ��Ͷ�Ͱ����w��DR�����ӄ��ȡ�MAO-B ���Ƅ��е�˾�����m + �S���� E��DATATOP������ɳ���m��ADAGIO���R��ԇ���ܾ����Ӿ������Mչ�����ã�DR ���ӄ��е��������� CALM-PD �о����_ƥ���_ REAL-ET �о���ʾ����ܾ��м���������á�������1200mg/d���oø Q10 ���R��ԇ�Ҳ��ʾ����ܾ��м���������á�
2.1.1 ���xˎ��ԭ�t���D 1��
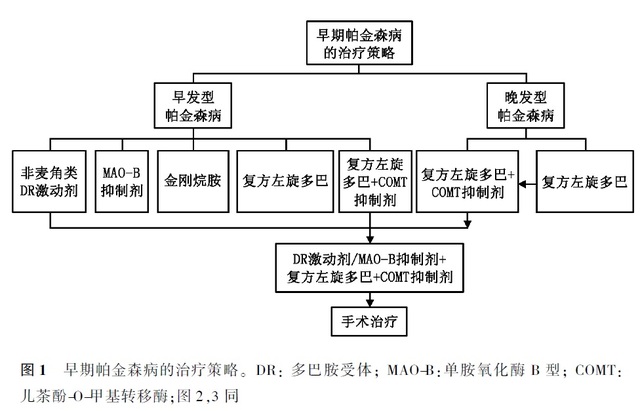
1. ��l�ͻ��ߣ��ڲ��������ܜp�˵���r�£����������x��
������� DR ���ӄ���
MAO- ���Ƅ���
�����鰷��
�ͷ�������ͣ�
�ͷ�������� + ����� -O ���D��ø��COMT�����Ƅ���
���xˎ�ﲢ�ǰ�����������������ͬ���ߵľ��w��r���x��ͬ�������������������W���ί�ָ�ϑ����x�����١��ڻ�ݣ����������ڽ���ԭ���ܳ��ܸ߃r���ˎ��t�����x�����ۣ����������֮�裬�����@�������\�ӰY�����F�J֪���ܜp�ˣ��t�����x�����ܻ�ݣ�Ҳ����С�������÷����١��ڻ�ەr��ͬ�rС�����ϑ��÷����ܡ�����������@������������ɭ��ˎ�ﯟЧǷ�ѵ���r�£����x�ÿ�đ�A��ˎ���籽������benzhexol����
���l�ͻ��а����ܜp�˵Ļ��ߣ�һ�����x�ͷ���������ί����S���Y��ļ��أ���Ч�p�˕r������ DR ���ӄ���MAO-B ���Ƅ��� COMT ���Ƅ��ί����M�������ÿ�đ�A��ˎ�����ᘌ��������Ի��ߣ���������^��ĸ����á�
2.1.2 �ί�ˎ�� ��đ�A��ˎ��Ŀǰ������Ҫ���ñ������������� 1~2mg��3 �� /d����Ҫ�m���ڰ�����Ļ��ߣ������o��Ļ��߲����]���á��� <60 �q�Ļ��ߣ�Ҫ��֪�L�ڑ��ñ��ˎ����ܕ��������J֪�����½�������Ҫ���ڏͲ��J֪���ܣ�һ���l�F���ߵ��J֪�����½��t������ͣ�ã���≥60 �q�Ļ�����ò����ÿ�đ�A��ˎ���M�����������ǰ���ٷʴ����߽��á�
�����鰷�������� 50~100mg��2~3 �� /d��ĩ�Α������� 4 �rǰ���á����لӡ���ֱ������и������ã����Ҍ����Ʈ��ӰY�Ў�����C ���C�������I���ܲ�ȫ���d�B������θ�������β��������ã������ڋDŮ���á�
�ͷ�������ͣ��S�z��������͡����ȶ��������ͣ�����ʼ������ 62.5~125.0mg��2~ �� /d�������������u���ӄ�������Ч�M��Ͳ����F�����õ��m�˄����S�֣���ǰ 1h ��ͺ� 1.5h ��ˎ��
�����������M�������t���ã�������ڑ��Õ��T�l���ӰY���F���C����ʾ���ڑ���С������≤400mg/d���������Ӯ��ӰY�İl�����ͷ�������ͳ�ጄ�������Ч������c������ጄ����оS�֕r�g�����L������Ч�����������öȵͣ���ʹ�Õr�������� 2 �N��ͬ�����D�Q�r�����ע�⡣��������������������ã��M��������ۡ������߽��á�
DR ���ӄ���Ŀǰ����Ƴ������� DR ���ӄ������xˎ������m������l������ɭ�����ߵIJ��̳��ڡ���飬�@��L��˥���Ƅ��ܱ��⌦�y���wͻ�|��Ĥ�� DR �a��“�}�_”�Ӵ̼����Ķ��A����p���\�Ӳ��l�Y�İl�������ӄ�������С�����_ʼ����u���ӄ������@�ÝM�⯟Ч�������F�����Þ�ֹ��
DR ���ӄ��ĸ������c�ͷ�����������ƣ���֮ͬ̎�����İY��Ӻͮ��ӰY�l���ʵͣ����wλ����Ѫ�����_��ˮ�[�;��������X��ʳ�����M���������M�ȣ��İl�����^�ߡ�DR ���ӄ��� 2 �N��ͣ�����������[ͤ��bromocriptine����������أ�pergolide����a- ���������[ͤ��dihydroergocryptine�����������֣�cabergoline�����������壨lisuride�����������������������pramipexole�����_ƥ���_��ropinirole������ؐ�ؠ���piribedil�����_���͡��rotigotine���Ͱ����ȣ�apomorphine��������� DR ���ӄ��Ɍ������K��Ĥ��׃�ͷ���Ĥ�w�S������ˣ�Ŀǰ�Ѳ�����ʹ�ã�������������ڇ�����ͣ�á�
Ŀǰ�������ж���ķ������ DR ���ӄ��У�
��ؐ�ؠ���ጄ�����ʼ������ 50mg��ÿ�� 1 �Σ��a�����������߿ɸĞ� 25mg��ÿ�� 2 �Σ��� 2 ������ 50mg��ÿ�� 2 �Σ���Ч������ 150mg/d���� 3 �οڷ�������������^ 250mg/d��
������������ 2 �N���ͣ���ጄ��;�ጄ�����ጄ����÷�����ʼ������ 0.125mg��ÿ�� 3 �Σ����e�a�����������߄t�� 1~2 �Σ���ÿ������ 0.125mg��ÿ�� 3 �Σ�һ����Ч������ 0.50~0.75mg��ÿ�� 3 �Σ�����������^ 4.5mg/d����ጄ����÷���ÿ�յĄ����c��ጄ���ͬ������ÿ�� 1 �η��á�
�������еķ������ DR ���ӄ��У�
�_ƥ���_����ʼ������ 0.25mg��ÿ�� 3 �Σ�ÿ������ 0.75mg ��ÿ�� 3mg��һ����Ч������ÿ�� 3~9mg���� 3 �η��ã�����Մ����� 24mg��
�_���͡����ʼ���� 2mg��ÿ�� 1 �Σ�ÿ������ 2mg��һ����Ч�������ڻ��ߞ�ÿ�� 6~8mg�������ڻ��ߞ� 8~16mg��
�������ж��������� DR ���ӄ��У�
���[ͤ�� 0.625mg��ÿ�� 1 �Σ�ÿ�� 5 ������ 0.625mg����Ч���� 3.75~15.00mg/d���� 3 �οڷ���
a- ���������[ͤ�� 2.5mg��ÿ�� 2 �Σ�ÿ�� 5 ������ 2.5mg����Ч���� 30~50mg/d���� 3 �οڷ������� 5 �Nˎ��֮�g�Ą����D�Q�飺��ؐ�ؠ��������������_ƥ���_�����[ͤ��α- ���������[ͤ =100��1��5��10��60�������w��H���酢����
MAO-B ���Ƅ�����Ҫ��˾�����m��selegiline������ɳ���m��rasagiline��������˾�����m�г�ጄ��Ϳ�ǻ�Ĥ���℩��˾�����m����ጄ������÷��� 2.5~5.0mg��ÿ�� 2 �Σ����糿��������ã����ڰ��������ϑ��ã���������ʧ�������c�S���� E2000U ���ã�DATATOP ����������ǻ�Ĥ���℩�����ա����á���ȫ�Ծ�����˾�����m��ጄ��������� 1.25~2.50mg/d����ɳ���m�������� 1mg��ÿ�� 1 �Σ��糿���á�θ���������ã����c 5- �uɫ���ٔzȡ���Ƅ���SSRI�����á�
COMT ���Ƅ����ڼ����������x�ͷ�������� +COMT ���Ƅ������������p���Ƭ����������� / ������� / ���ȶ�͏ͺ��Ƅ�����������̈́�����ͬ�ֳ� 4 �N���ͣ��ί������H���Ը��ƻ��߰Y������п����A�������t�\�Ӳ��l�Y�İl����
�� FIRST-STEP �� STRIDE-PD �о���ʾ���������p������ڑ��ò��������t�\�Ӳ��l�Y�����Ӯ��ӰY�l���Ď��ʣ�Ŀǰ�д栎�h���д��Mһ������C��
�ڼ��������ڣ����Ïͷ�������ͯ�Ч�p�˕r�������Ӷ��п���entacapone�����п���tolcapone���ί����_���Mһ�����ưY������á����п���������ÿ�� 100~200mg�����ôΔ��c�ͷ����������ͬ����ÿ�շ��Ïͷ�������ʹΔ��^�࣬Ҳ�����ڏͷ�������ʹΔ������c�ͷ��������ͬ�������ßoЧ���п���ÿ�������� 100mg��ÿ�� 3 �Σ���һ���c�ͷ��������ͬ�����˺��g�� 6h ���ã����Ԇ��ã�ÿ��������� 600mg��
��ˎ�︱���������a���^ʹ���ູ���ڸɡ��D��ø���ߡ���ʹ����ɫ׃�S�ȡ��п�����ܕ����¸ι��ܓp��������ܱO�y�ι��ܣ���������ˎ֮���ǰ 3 ���¡�
2.2 ����������ɭ�����ί�
����������ɭ������������������ɭ�����R�����F�O����s�������м����������Mչ��Ҳ��ˎ�︱���û��\�Ӳ��l�Y�������c���С�������������ɭ�����ߵ��ί���һ����Ҫ�^�m������ƻ��ߵ��\�ӰY���һ����Ҫ����̎��һЩ�\�Ӳ��l�Y�ͷ��\�ӰY�
2.2.1 �\�Ӳ��l�Y���ί�
�\�Ӳ��l�Y���Y��Ӻͮ��ӰY��������ɭ�������ڳ�Ҋ�İY��{��ˎ��N���������ˎ�Δ����Ը��ưY����g�ί����X�늴̼��g��DBS�����Я�Ч��
�Y��ӵ��ί����D 2�����Y�����Ҫ������ĩ������endofdosedeterioration�����_ - �P�F��on—ffphenomenon��������ĩ������̎�������飺
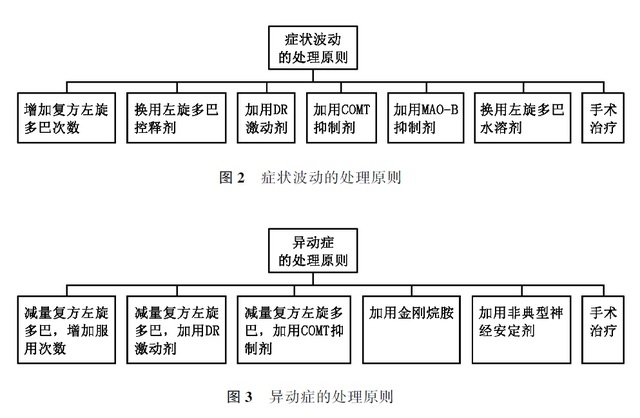
2. ���ӰY���ί����D 3�������ӰY��AIMs���ַQ���\���ϵK��dyskinesia�����������宐�ӰY���p�ஐ�ӰY�ͼ������ϵK��dystonia����
�����宐�ӰY��̎�������飺
�p��ÿ�Ώͷ�������͵Ą�����
�������dž��Ïͷ�������ͣ����m���p�ل�����ͬ�r���� DR ���ӄ�������� COMT ���Ƅ���
���ý����鰷��C ���C������
���÷ǵ��Ϳ�����ˎ���ȵ�ƽ��
��ʹ�Ïͷ�������Ϳ�ጄ����t���Q�ó�ጄ��������ጄ����۷eЧ����
���p�ஐ�ӰY�������������ӰY�̈́�ĩ���ӰY����̎�������飺
����ʹ�Ïͷ�������Ϳ�ጄ����Q�ó�ጄ�����ÓQ��ˮ�܄���������Ч���℩�����ӰY��
�����L��˥�ڵ� DR ���ӄ������L�������Ѫ�������˥�ڵ� COMT ���Ƅ������Ծ��℩ĩ���ӰY��Ҳ���������ڸ��Ƅ������ӰY�������mݔע DR ���ӄ���������ͼ�������������ͬ�r���Ʈ��ӰY�ͰY��ӣ�Ŀǰ����ԇ�ڷ��Ƅ��Ƿ����_��ͬ��Ч���������ί����ӰY��ˎ���������ڻ����� DA �ܵ����� A2A ���w�������ί�Ч�������P�R��ԇ������_չ��
���������ϵK��̎�������飺
˯ǰ���Ïͷ�������Ϳ��Ƭ���LЧ DR ���ӄ���������ǰ���Ïͷ�������ͳ�ጄ���ˮ�܄�����“�_”�ڼ������ϵK��̎������ͬ���宐�ӰY�����g�ί���ʽ��Ҫ�� DBS���ɫ@���档
�����ӷ��Ïͷ�������͵�ÿ�տ����������m������ÿ�շ�ˎ�Δ����p��ÿ�η�ˎ��������������Ч�����\�ӰY���ǰ�ᣩ�����m������ÿ�տ�������ԭ�Є����������r�£���ÿ�η�ˎ������׃�������ӷ�ˎ�Δ���
�ɳ�ጄ��Q�ÿ�ጄ������L������͵����Õr�g�����m�������ڳ��F��ĩ����������l����ҹ�g�r���^���x���������� 20%~30%������ָ���J�鲻�ܿs��“�P”�ڣ��� C ���C������Ӣ�� NICE ָ�����]�������ڻ����Б��ã������������x���� B ���C������
�����L��˥�ڵ� DR ���ӄ������������������_ƥ���_�� B ���C�����������֡������Ȟ� C ���C�������[ͤ���ܿs��“�P”�ڣ��� C ���C���������� DR ���ӄ�����Ч�p�˿ɇLԇ�Q����һ�N DR ���ӄ���
���Ì��y���w�a�����m�� DA �ܴ̼��� COMT ���Ƅ������ж��п���� A ���C�����п���� B ���C����
���� MAO-B ���Ƅ���������ɳ���m�� A ���C����˾�����m�� C ���C����
�����ʳ���������|��������������ռ�ͨ�^Ѫ�X���ϵ�Ӱ푣����ڲ�ǰ 1h ��ͺ� 1.5h ��ˎ���{�������ʳ������Ч��
���g�ί���Ҫ�����X�ˣ�STN���� DBS �ɫ@���棬�� C ���C�������_ - �P�F���̎���^�����y�������x�ÿڷ� DR ���ӄ�����ɲ��������mݔע������ͼ����������� DR ���ӄ�������������ȣ���
2.2.2 �˄�ƽ���ϵK���ί�
�˄�ƽ���ϵK������ɭ������ˤ�ӵ��Ҋԭ������׃�Q�wλ���D���������͏����r�l����Ŀǰȱ����Ч���ί���ʩ���{��ˎ���������ˎ��ż����Ч�������{�����w���ġ�̤���ߡ����ߡ� ��� �����������������Խ���w���挍�Ļ����ģ��ȿ������档��Ҫ�rʹ������������݆�Σ����÷��o��
2.2.3 ���\�ӰY����ί�
����ɭ���ķ��\�ӰY���漰�S����ͣ���Ҫ�������X�ϵK�������ϵK�����������ϵK��˯���ϵK����o��e�O���������ί���
�����ϵK���ί����Ҋ�ľ����ϵK���������ͣ����]�����X���J֪�ϵK��V���ȡ�������Ҫ��e���ߵľ����ϵK���ɿ�����ɭ��ˎ���T�l��߀���ɼ������팧�¡�
����ǰ�߄t��������T�l���߾����ϵK�Ď��ʶ�������p��ͣ�����¿�����ɭ��ˎ���đ�A��ˎ�������鰷��MAO-B ���Ƅ� DR ���ӄ�������ȡ���ϴ�ʩ���ߵİY����Ȼ���ڣ��ڲ����@��������ɭ�����\�ӰY���ǰ���£��Ɍ��ͷ���������p����
���ˎ���{��Ч�������룬�t��ʾ���ߵľ����ϵK���ܞ鼲�����팧�£���Ҫ���]���Y��ˎ��ᘌ����X��������ί������]�x���ȵ�ƽ��clozapine�������ƽ��quetiapine����ǰ�ߵ������ԏ��ں��ߣ������ȵ�ƽ���� 1%~2% �Ď��ʌ���������ȱ���Y������O�yѪ����Ӌ����
���������ͣ����]���ί����ɑ����x���� SSRI��Ҳ�ɑ��� DR ���ӄ������������������ȿ��Ը����\�ӰY�ͬ�rҲ�ɸ��������Y�����������lorazepam���͵������������Ǡ�Bʮ����Ч��
ᘌ��J֪�ϵK�ͰV�����ί����ɑ���đ�A��ø���Ƅ���������˹����rivastigmine�����������R��donepezil���ȣ��Լ���������mementine������������˹�����C���^���֡�
���������ϵK���ί����Ҋ�����������ϵK�������ء������ϵK��λ���Ե�Ѫ���ȡ����ڱ��أ��z������Һ�w��ˮ�����߲ˡ��w�S�غ�����ǣ�10~20g/d���������غ͵Č��aˎ���ܸ��Ʊ��ذY�������ǣ�lactulose�������C�衢���SƬ�����a�~�ȣ�Ҳ�ɼ���θ���ˎ���������ͪ��Īɳ�����ȡ���Ҫͣ�ÿ�đ�A��ˎ�������\�ӡ�
�������ϵK�е����l���ͼ�������ʧ�����ί����ɲ������ܿ�đ�A��ˎ����W��������oxybutynin���������̫�֣�propantheline���������_����tolterodine����ݹ�ЉA��hyoscyamine���ȡ�
�������o�����߄t�o��đ�A���Ƅ����������ã������������ɭ�����\�ӰY��������F������������ȡ�gЪ���坍��������ǰ���������ʴ����𣬇����߱�Ҫ�r����λ���Ե�Ѫ�����ߑ������}��ˮ�Ĕz������
˯�ߕŗ���^λ����Ҫƽ�ɣ��ɴ�����ѝ����Ҫ���ٵ؏��Pλ����λ���������x a- �I�������ܼ��ӄ������midodrine���ί����ү�Ч��ѣ�Ҳ��ʹ���x�������ܶ�Ͱ����w����������ͪ��
˯���ϵK���ί���˯���ϵK��Ҫ����ʧ�ߡ������ۄ���˯���О鮐����RBD���������^����˯��EDS����ʧ���Ҋ�Ć��}��˯�߾S�����y���ַQ˯�����飩���l���X�ѿ���ʹ������ڜ\˯�����ٴγ��F���������ڰ�����õĶ�Ͱ���ˎ������ҹ�g�ѺıM������ҹ�g�\�Ӳ��ܶ����·������y������ҹ�����ࡣ
����cҹ�g������ɭ���Y�����P������������Ϳ�ጄ���DR ���ӄ��� COMT ���Ƅ��t����Ч��������ڷ���˾�����m������鰷�������ڰ��������ߣ�������m����ˎ�r�g��˾�����m�����糿��������ã������鰷�������� 4 �cǰ���ã����o���@���ƣ��t��p������ͣˎ�����x�ö�Ч����o����ˎ��
�� RBD ���߿�˯ǰ�o������������һ�� 0.5mg ������Ч��EDS �����c����ɭ���ć��س̶Ⱥ��J֪���ܜp�����P��Ҳ���c������ɭ��ˎ�� DR ���ӄ���������͑������P�����������ÿ�η�ˎ����F��˯���t��ʾˎ���^��������ˎ�p���������ڸ��� EDS��Ҳ����������Ϳ�ጄ����泣ጄ������ܕ������ڱ����p�p��ˎ����˯��
���X�ϵK���ί����Ҋ�ĸ��X�ϵK��Ҫ�������X�p�ˡ���ʹ����ľ�������ȾC������RLS�������X�p��������ɭ���������ஔ��Ҋ���Ҷ�l�����\�ӰY����F֮ǰ���꣬����Ŀǰ�Пo���_��ʩ�܉�������X�ϵK��
��ʹ����ľ������ɭ����������������ɭ�������б��^��Ҋ���������伲������Ҳ�����ǰ��S���P����׃���£����������ɭ��ˎ���ί�“�_��”��ʹ����ľ�p�p����ʧ��“�P��”�ͬF���t��ʾ������ɭ�����£������{���ί������L“�_��”����֮���t����������������ԭ�����𣬿����x���������ί���ʩ��
������ RLS ������ɭ�����ߣ�����˯ǰ 2h ���x�� DR ���ӄ������������ί�ʮ����Ч����o��ͷ��������Ҳ����Ч��
3. ���g��
����ˎ���ί��@Ч���@�����L���ί��į�Ч���@�p�ˣ�����F���ص��\�Ӳ��Ӽ����ӰY�߿ɿ��]���g�ί���ԔҊ�Ї�����ɭ���X�늴̼��������ҹ��R����Ҫ���{�������g�������@�����\�ӰY������ܸ��μ������g�����葪��ˎ���ί������������p�ل�����
���g������������m���C����ԭ�l������ɭ��������ɭ�B�ӾC�������������g�Ľ����C�����g��֫�w��ͣ�����ֱ���^�õį�Ч�������|�w�����S�Y�����˄�ƽ���ϵK�t�o���@��Ч��
���g������Ҫ�����˚��p�g�� DBS��DBS ���������o������ȫ�Ϳ��{���Զ�������Ҫ�x�����g���c�����n����ȂȲ���GPi�������X�����g�ˣ�VIM�������X�ˣ�STN���������� STN �� DBS �����������ֱ���\���t���ͮ��ӰY�į�Ч����@����
�gǰ������������п����� STNDBS �ί���Ӌ�A���ָ�ˣ�B ���C���������g�Ͳ��̿����� STNDBS ��Ӌ�A���ָ�ˣ����̶̵����p���߿����^�����L�����g��Ļ����g����Ƹ������@��C ���C������Ȼ���Пo����C���� GPi �� VIMDBS ���A�����������κν��h��U ���C������
4. �����c�\�ӯ���
�����c�\�ӯ���������ɭ���Y��ĸ����������Ӿ����̵��Mչ���ܶ���һ���Ď���������ɭ�����߶���ڲ��B�ϵK���˄�ƽ���ϵK���Z�Ժͣ��������ϵK�ȣ����Ը�����ͬ���Є��ϵK�M�������Ŀ��ͻ��\��Ӗ����
�罡���١�̫�Oȭ�����ܵ��\�ӣ��M���Z���ϵKӖ�������BӖ�����˄�ƽ��Ӗ���ȡ�����ÿ�ՈԳ֣��t����������ߵ��������������������\�ӹ��ܣ��������Lˎ�����Ч�ڡ�
5. �����茧
����ɭ�����߶���������������ϵK���������l��������ɭ���\�ӰY����Fǰ�ͳ��F֮����Ӱ푻��������|������ҪΣ�U����֮һ��ͬ�rҲ��Ӱ푿�����ɭ��ˎ���ί�����Ч�ԡ���ˣ�������ɭ�����ί����H��Ҫ�Pע���ƻ��ߵ��\�ӰY�����Ҫ��ҕ���ƻ��ߵ������������ϵK��������Ч�������茧�Ϳ�����ˎ���ί����أ��Ķ��_�����M����ί�Ч����
6. �����o��
������ɭ�����߳��ˌ��I�Ե�ˎ���ί����⣬�ƌW���o�팦�S�ֻ��ߵ������|��Ҳ��ʮ����Ҫ�ġ��ƌW���o������������Ч���Ʋ��顢���ưY����һ�����o���ί����ã�ͬ�rҲ�܉���Ч�ط�ֹ�`��������ȿ��������¼��İl����
��֮������ɭ�����ί��]�н^���Ĺ̶�ģʽ����鲻ͬ����֮�g�İY����ܕ����څ^�e�����ί������ж�Ҳ����һ�������ͬ���ߌ��ί���������ڲ�ͬ��ͬһ�����ڲ�ͬ�����A�Ό��ί�������Ҳ���M��ͬ��
��ˣ���ָ�Ͽ����m����һ��Ҏ�ɣ����R�����H���Õr����ע��Ԕ���˽�ߵIJ��飨�������س̶ȡ��Y����͵ȣ����ί�������r���Ƿ���Ч����Ч�r�g�����þS�֕r�g��“�_��”���L��“�P��”�s�̕r�g���Пo�����ûl�Y���ȣ��Y�����Լ����ί�������ѭָ�ϣ����w�F���w��ԭ�t�������_������������ί�Ч����
�������ߣ����A�t�W�����W�֕�����ɭ�����\���ϵK�W�M
����ժ�ԣ������A���s־��2014 �� 6 �� �� 47 �� �� 6 �� P428-433
TAG���Ї�����ɭ���ί�ָ��
���PˎƷ

�ƌ���
�����T����
���TˎƷ
- �f�ٻ��L��
- ·����
- ��̩
- �w��
- ��̩̹
- ��̹
- ����ܛ�z��
- ���`��
- ����ͨ���z��
- �X��ͨ��
- �䌚��
- ����ͨ
- ��˼��
- �����������Aע��Һ
- ����
- ���ɱ�
- �ͷ������ۭh����Ƭ
- ����������
- ���Z
- �}�ᱽ����Ƭ
- ������
- ��˼�_
- �쵤ͨ�j�z��
- �Ӱ͇���Ƭ
- ��ʮ��ζ������
��ˎƷ
- �\����Ԫ�� |
- �X���L���z�Y |
- �����V�� |
- ����ɭ�� |
- �d�B |
- ���X�c |
- ƫ�^ʹ |
- �p�� |
- ��l��Ӳ���Y |
- ������ʹ |
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
�ٝ�ˎ���Y�|- ��I���ˠI�I���� | ���WˎƷ��Ϣ�����Y���C







